此前一项研究发现,62% 的男性和 46% 的女性都希望自己能长得更高。儿童和青少年时期的骨骼成长对成年后身高和骨骼健康至关重要,因此,确保儿童达到其遗传潜能的最大生长成为了该领域的核心目标。
众所周知,有很多外部和可调控因素,如钙、维生素D的摄入,以及运动,都会影响骨骼发育。其中,体育锻炼或运动训练可以通过增强骨骼质量和强度,最终改善骨骼形成。
值得注意的是,锻炼的时间安排(exercise timing)被认为是影响锻炼生理结果的重要变量之一。一天中不同时间的锻炼效果可能不同,因此在设计运动干预措施时需要考虑这一因素。
例如,一项随机交叉临床试验显示,在改善2型糖尿病患者的血糖水平方面,下午锻炼比上午锻炼更有效。尽管如此,运动如何具体影响骨骼生长及其内在机制仍需深入探索。
骨骼的生长主要依赖于生长板中的两个关键区域——增生带和肥厚带中软骨细胞的活动。这些软骨细胞负责构建和组织细胞外基质,是骨骼形成和延长的基础。在胚胎期及出生后,这些细胞经历营养摄取用和能量消耗的周期波动。如果葡萄糖氧化减少,会导致能量供应不足,限制细胞增殖、影响蛋白质正确折叠并减少胶原蛋白的产生,而三羧酸循环中ATP的合成受阻会影响软骨细胞的成熟。
运动对于骨骼新陈代谢和全身能量平衡至关重要,能激活AMPK和sirtuin等分子机制,协同调节细胞代谢以适应运动需求,这些过程受生物钟调控,表现出昼夜节律性波动。因此,运动的时间可能产生不同的生理适应,研究其对骨骼生长的具体时段效应有助于最大化生长潜力的优化。
在一项新的研究中,来自中国华中科技大学的研究人员进行了一项创新研究,探索小鼠在不同时间段运动对其骨骼生长影响的差异。研究发现,小鼠在一天中的早晨(相当于人类活动早期)进行运动后,骨骼的长度和质量增长得更快。高通量的基因表达和代谢分析揭示,早晨运动能激活与骨骼生长相关的基因,同步骨骼代谢的昼夜节律,并且通过促进氧化磷酸化过程加速骨骼生长。
值得注意的是,一种称为5-氨基咪唑-4-甲酰胺(5-aminoimidazole-4-carboxamide ribonu-cleoside, AICAR)的氧化磷酸化激活剂能有效增加骨骼长度和质量。这些发现共同为增强骨骼健康提供了宝贵的见解,并可能具有重要的治疗意义。
相关研究结果于2024年5月28日在线发表在Nature Metabolism期刊上,论文标题为“Time of exercise differentially impacts bone growth in mice”。论文通讯作者为华中科技大学同济医学院附属协和医院的陈莉莉(Lili Chen)教授。
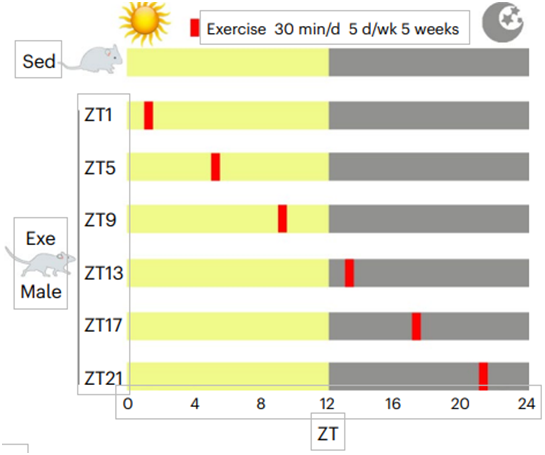
小鼠的昼夜活动可分为活跃期(active phase)和休息期(rest phase),其中活跃期为ZT12-ZT24,休息期为ZT0-ZT12
图片来自Nature Metabolism, 2024, doi:10.1038/s42255-024-01057-0
这项新的研究结果强调了确定理想锻炼时间的重要性,这样可以通过运动训练最大限度地发挥锻炼对骨骼健康的积极影响。
为了研究锻炼对骨骼代谢和骨健康的影响,研究人员在锻炼前 5 分钟给小鼠髓内注射寡霉素 A(oligomycin A),并分析不同时间段的锻炼效果。他们的研究结果表明,在活跃期早期进行锻炼会促进氧化磷酸化和TCA循环,而在休息期进行锻炼会刺激糖酵解。氧化磷酸化在活跃期早期被锻炼激活,为软骨细胞增殖和基质沉积等高能量活动提供丰富的 ATP,进一步为其增殖、分化和细胞外基质形成提供充足的能量。而与此相反,糖酵解产生的 ATP 比氧化磷酸化少,这表明休息期锻炼在促进骨骼生长方面的效果可能较差。
此外,时间高通量转录组学分析显示,活跃期早期的锻炼会增强骨骼生长相关基因的表达,并诱导骨骼发育和碳水化合物代谢相关基因的昼夜节律振荡。并且,核心昼夜节律转录机制在活跃期早期的锻炼后继续振荡,而Bmal1在休息期(rest phase)的锻炼后几乎没有发生节律性表达。这些发现支持了之前的证据,即锻炼是骨骼系统生物钟功能的有效调节剂。
值得注意的是,研究发现,在一天中的活跃期早期进行锻炼能够维持身体原本的生理节律性表达模式,这种模式在久坐者身上尤为明显。相反,如果选择在休息期进行锻炼,则可能会扰乱这种自然的生理节律性表达模式。这些观察结果提示我们,遵循并保持身体的自然节律性表达节奏对于骨骼健康是有益的。不过,当前的研究受限于样本采集的频率,研究团队还无法精确描绘出每天的详细节律性转录组变化,这意味着未来的研究可能需要更密集的采样和更细致的时间跟踪,以揭示出每日节律变化的精细模式。
综上所述,该研究不仅强调了锻炼时机对骨骼健康的重要性,还为未来开发针对特定代谢途径的治疗手段提供了科学依据。
参考资料:
Shaoling Yu et al. Time of exercise differentially impacts bone growth in mice. Nature Metabolism, 2024, doi:10.1038/s42255-024-01057-0.
更多阅读: